Frage von Dr. A.H. aus Berlin: >> Welche Bedeutung wird heute in der Behandlung des schweren steroidpflichtigen Asthma bronchiale einer zusätzlichen immunsuppressiven Therapie mit Methotrexat beigemessen? << Antwort: >> Methotrexat (MTX), ein Zytostatikum, das in hohen Dosen (50-150 mg/Woche) eine Hemmung der Dihydrofolatreduktase bewirkt, wird seit 1948 in der Behandlung akuter Leukämien eingesetzt. In niedriger Dosierung (5-25 mg/Woche) hat es mittlerweile auch als Basistherapeutikum in der Behandlung der Psoriasis-Arthropathie und der Rheumatoiden Arthritis (vgl. 14) einen festen Platz. Der genaue pharmakologische Angriffspunkt von MTX in niedriger Dosierung ist jedoch bis heute nicht völlig geklärt. Diskutiert werden neben einer lmmunsuppression auch antientzündliche Effekte.
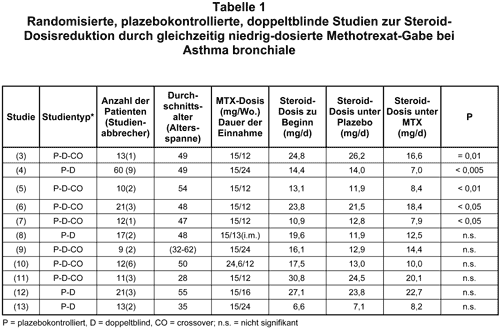
Erste Beobachtungen an Patienten mit schwerem steroidpflichtigem Asthma bronchiale, bei denen durch eine zusätzliche Gabe von niedrig-dosiertem MTX eine deutliche Dosisreduktion der oralen Kortikosteroide erzielt werden konnte, waren vielversprechend (2, 3). Bis heute wurden zum Thema „MTX und Asthma“ über 90 Artikel verfaßt. Beschränkt man sich bei kritischer Durchsicht auf randomisierte, plazebokontrollierte, doppeltblinde Versuchsreihen, finden sich elf Studien (3-13) und eine Metaanalyse (14). Eine Übersicht über diese Studie gibt Tab. 1.
Eingeschlossen wurden Patienten, deren Asthma bronchiale mit der konventionellen Therapie (Theophyllin, inhalative Kortikosteroide und inhalative Beta-Agonisten) alleine nicht mehr beherrschbar war und eine zusätzliche Dauermedikation mit systemischen Kortikosteroiden erforderte. Die durchschnittliche Ausgangsdosis Prednison/Prednisolon vor Einschluß ins Studienprotokoll schwankt zwischen den einzelnen Patienten und Studien erheblich zwischen 6,6 mg und 30,8 mg/d. Mit einer Ausnahme (10) wurde den Patienten Methotrexat in einer Dosis von 15 mg/Woche verabreicht. Die Patienten wurden unter der Einnahme von MTX oder Plazebo angeleitet, ihre orale Steroidmedikation stufenweise soweit zu reduzieren, wie dies unter Erhaltung eines klinisch stabilen Zustandes möglich war.
Die meisten der Studien untersuchten die Auswirkungen der Methotrexat-Gabe über einen Zeitraum von drei bis vier Monaten. Drei der Studien (4, 9, 13) berücksichtigten auch längerfristige Effekte (6 Monate). Alle Patienten erhielten während der gesamten Studiendauer weiterhin zusätzlich ihre reguläre Asthmatherapie.
Mit einer Ausnahme (4) wurden alle Studien mit einer Patientenzahl von 21 oder weniger Patienten durchgeführt. Insgesamt wurde ein Kollektiv von 233 Patienten in die Studien einbezogen. 199 Patienten vollendeten die Behandlung, 34 Patienten brachen die Medikamenteneinnahme aus unterschiedlichen Gründen vorzeitig ab und wurden in der statistischen Auswertung nicht berücksichtigt.
Sechs der elf Studien (8-13) kommen zu dem Schluß, daß die zusätzliche Einnahme von Methotrexat nicht zu einer signifikanten Dosisreduktion der Kortikosteroide führt. Eine Metaanalyse der Ergebnisse, die im Juli 1997 in Chest veröffentlicht wurde (14), zeigt jedoch das Gegenteil. Der Autor berechnet unter Berücksichtigung aller bislang erhobenen Daten, daß sich durch die Einnahme von Methotrexat der durchschnittliche Steroidverbrauch statistisch signifikant um 4,37 mg/d, d.h. um 23,7%, senken läßt. Dieses Ergebnis beruht im wesentlichen auf der insgesamt höheren Patientenzahl der Studien, die die Möglichkeit zu einer signifikanten Dosisreduktion aufzeigten bzw. der Studie von Shiner, R.J., et al. (4), der 60 Patienten einschloß und besonders kritisch beobachtete. Das von Mann, M.G. (14), vorgelegte Ergebnis war auch bei einer Analyse sieben verschiedener Untergruppen reproduzierbar.
Weiterhin zeigte sich, wenn auch ohne statistische Signifikanz, die Tendenz, daß eine längere Einnahmedauer von MTX eine größere Dosisreduktion bewirkt. Ebenso scheinen Patienten mit einer niedrigeren Ausgangsdosis einen größeren Effekt in der Dosisreduktion zu erzielen.
Als Nebenwirkungen von Methotrexat (vgl. 14) wurden in einigen Fällen Übelkeit, Erbrechen, Bauchschmerzen, Durchfall, Ulzera der Mundschleimhaut, leichter Haarausfall, Kopfschmerzen sowie eine meist geringfügige Erhöhung der Transaminasen beschrieben. In zwei Studien kam es bei fünf von 38 (4) bzw. bei drei von elf (9) Patienten zu einem Anstieg der Leberenzyme auf mehr als das Dreifache des Ausgangswertes, was zum Abbruch der MTX-Einnahme führte. In keiner der Studien traten lebensbedrohliche oder irreversible Nebenwirkungen von Methotrexat auf.
Fazit: Die Gabe von Methotrexat in niedriger Dosierung führt bei Patienten mit schwerem steroidpflichtigem Asthma bronchiale zu einer Dosisreduktion der oralen Kortikosteroide. Dieser Effekt ist in Studien mit einer Einnahmedauer von 24 Wochen und einem Protokoll, das vor Beginn der MTX-Einnahme eine Minimierung der Steroidtherapie einfordert, am größten. Nebenwirkungen scheinen unter niedrig-dosiertem MTX in Ausprägung und Häufigkeit moderater und insgesamt seltener als unter einer Dauermedikation mit Steroiden. Unsicher bleibt hier die Häufigkeit des Auftretens unter einer prolongierten Einnahme von Methotrexat. MTX sollte daher nur bei Patienten, deren Asthma langfristig (> 6 Monate) nur durch Gabe hochdosierter Steroide (> 15 mg/d) kontrolliert werden kann, unter strenger klinischer Kontrolle versucht werden. << Literatur
1. AMB1996, 30, 73.
2. Mullarkey, M.F., et al.: Ann. Allergy 1986, 56, 347.
3. Mullarkey, M.F., et al.: N. Engl. J. Med. 1988, 318, 603.
4. Shiner,R.J., et al.:Lancet 1990, 336, 137.
5. Dyer, P.D., et al.: J. Allergy Clin. Immunol. 1991, 88, 208.
6. Stewart, G.E., et al.: J. Allergy Clin. Immunol. 1994, 94, 482.
7. Hedman, J., et al.: Eur. J. Clin. Pharmacol. 1996, 49, 347.
8. Erzurum, S.C., et al.: Ann. Intern. Med. 1991, 114, 353.
9. Taylor, D.R., et al.: N. Z. Med. J. 1993, 106, 409.
10. Trigg, C.J., et al.: Respir. Med. 1993, 87, 211.
11. Coffey, M.J., et al.: Chest 1994, 105, 117.
12. Kanzow, G., et al.: Lung 1995, 173, 223.
13. Ogirala, R.G., et al.: Am. J. Respir. Crit. Care Med. 1995, 152, 1461.
14. Mann, M.G.: Chest 1997, 112, 29.