Zusammenfassung: Im Jahre 2003 sind 17 Medikamente neu zugelassen worden. Es handelt sich um sieben innovative Substanzen mit therapeutischer Relevanz (als Antiemetikum, zur Therapie von Speicherkrankheiten, der Akromegalie, der komplizierten Tibiafraktur, der fortgeschrittenen Osteoporose und von AIDS). Fünf Substanzen haben zumindest eine verbesserte Pharmakodynamik oder Pharmakokinetik. Fünf weitere Substanzen sind Molekülvariationen und als Analogpräparate ohne zusätzlichen Nutzen anzusehen. Der insgesamt geringe Anstieg des gesamten Umsatzvolumens ist auf deutliche Anstiege bei der Verordnung teurer Spezialmedikamente und Analogpräparate zurückzuführen. Präzise Indikationen und der kritische Vergleich der Preis/Leistungs-Verhältnisse können und müssen zu einer Entlastung des Arzneimittelbudgets führen. Nur so können die Kosten der Polymorbidität in höherem Lebensalter aufgefangen werden.
Im Oktober ist der Arzneiverordnungs-Report 2004 erschienen (1), der den Arzneimittelmarkt und das Verordnungsverhalten der Vertragsärzte der gesetzlichen Krankenversicherungen im Jahr 2003 zeigt und analysiert. Mit 749 Mio. Verordnungen wurde ein Arzneimittelumsatz von 24,1 Mrd. EUR erzeugt. Das ist erneut ein Anstieg gegenüber dem Vorjahr von etwa 6%, obwohl mehr Generika verordnet wurden und umstrittene Arzneimittel eine immer geringere Rolle spielen. Der Zuwachs kommt durch ein Umsatzplus von 14,2% bei den Spezialpräparaten und von etwa 20% bei den Analogpräparaten zu Stande. Spezialpräparate sind meist teuer und werden für besondere Therapieverfahren zunächst in Kliniken eingesetzt und von dort in die Ambulanz empfohlen (Transplantationsmedizin, Onkologie, AIDS-Therapie, Reproduktionsmedizin). Analogpräparate sind patentfähige Molekülvarianten meist ohne zusätzlichen Nutzen, die am Ende des Patentschutzes der Muttersubstanz auf den Markt gebracht werden. Im Folgenden wollen wir kurz die Arzneimittel vorstellen bzw. ins Gedächtnis rufen, die 2003 neu auf den Markt gekommen sind und werden sehen, dass es sich dabei meist um Spezial- oder Analogpräparate handelt.
Neue Medikamente 2003 (Tab. 1): Adalimumab (Humira®) ist ein neuartiger Antagonist des Tumor-Nekrose-Faktors alpha (TNF), der dem humanen Immunglobulin (IgG1) völlig entspricht und der in speziellen Situationen zur Behandlung der Rheumatoiden Arthritis zugelassen ist. Er hat eine im Vergleich zu Etanercept (Enbrel®) und Infliximab (Remicade®) deutlich verlängerte Halbwertszeit von 15-19 Tagen und muss daher nur alle 14 Tage injiziert werden. Trotzdem sind die Tagestherapiekosten höher als bei den beiden Vergleichssubstanzen. Einen Wirksamkeitsunterschied scheint es nicht zu geben. Die Substanzen sind aber nicht vergleichend getestet worden. Unerwünschte Arzneimittelwirkungen (UAW) sind bei allen: Aktivierung von Tuberkulose, Sepsis, Lymphome. Deswegen gilt für die ganze Gruppe der TNF-Antagonisten, was wir schon für Etanercept gesagt haben (2): Sie sollten als Basistherapeutikum nur bei unzureichender Wirkung von Methotrexat eingesetzt werden und nur im Rahmen von prospektiven Studien oder Registern.
Adefovirdipivoxil (Hepsera®) steht seit 2003 als drittes Medikament neben Interferon alfa und Lamivudin (Epivir®, Zeffix®; 3) zur Behandlung der Hepatitis B zur Verfügung. Es ist als Nukleosidanalogon nephrotoxisch und wurde daher – in höherer Dosierung – als HIV-Therapeutikum nicht weiter getestet. Zur Behandlung der Hepatitis B kommt es bei Lamivudin-Resistenz in Frage, denn Adefovir-Resistenz gibt es (noch) nicht. Die Kosten sind fünfmal höher als die von Lamivudin. Langzeitergebnisse zu Viruseradikation sowie Zirrhose- und Karzinomhäufigkeit fehlen. Das Präparat ist aber für einen kleinen Patientenkreis in der Hand des Spezialisten eine Bereicherung.
Aprepitant (Emend®) ist ein Arzneimittel mit neuartigem Wirkprinzip (Neurokinin-1-Rezeptor-Antagonist). Es ist zur Prävention von Übelkeit und Erbrechen, akut oder verzögert eintretend, bei hoch-emetogener Chemotherapie mit Cisplatin zugelassen. Aprepitant blockiert nach Bindung an Neurokinin-1-Rezeptoren die Wirkung des Neuropeptids (Neurotransmitters) Substanz P, die an der neuronalen Steuerung zahlreicher physiologischer Vorgänge, u.a. in Nerven und im Gehirn, beteiligt ist. Ihr wird in der Pathophysiologie des verzögert einsetzenden Erbrechens eine große Rolle zugeschrieben. In randomisierten klinischen Studien (meistens Vergleich 5-HT3-Rezeptor-Antagonist plus Dexamethason mit/ohne Aprepitant) konnte die antiemetische Wirksamkeit von Aprepitant vor allem beim verzögert einsetzenden Erbrechen nachgewiesen werden (5). Alleine oder in Kombination mit Dexamethason ist Aprepitant bei akutem Erbrechen deutlich weniger wirksam als die 5-HT3-Rezeptor-Antagonisten. Randomisierte klinische Studien, in denen die Wirksamkeit von Aprepitant mit der Standardtherapie des verzögerten Erbrechens (Dexamethason plus Metoclopramid oder Dexamethason plus 5-HT3-Rezeptor-Antagonist) verglichen wurden, liegen bisher nicht vor. Die Kombinationstherapie des Cisplatin-induzierten Erbrechens mit 5-HT3-Rezeptor-Antagonist (Tag 1), Dexamethason (Tage 1-4) und Aprepitant (Tage 1-3) wird durch Aprepitant um etwa 86 EUR/Chemotherapie-Zyklus verteuert. Die Indikation der neuen Substanz Aprepitant muss deshalb vor Verordnung streng geprüft werden. Aus der hepatischen Metabolisierung von Aprepitant (vorwiegend über CYP3A4) resultiert eine Vielzahl klinisch bedeutsamer Wechselwirkungen (siehe Fachinformation). Insgesamt ist Aprepitant eine interessante, wenn auch teure Bereicherung in der supportiven Therapie bei hoch-emetogenen, Cisplatin-haltigen Chemotherapie-Schemata.
Dutasterid (Avodart®) ist als Analogpräparat zu Finasterid (Propecia®, Proscar®) anzusehen. Finasterid hemmt die 5-alpha-Reduktase Typ 2, während Dutasterid zusätzlich das Isoenzym Typ 1 hemmt. Dadurch wird die Reduktion von Testosteron zu Dihydrotestosteron in der Prostata und in anderen Organen stark reduziert. Das Prostata-Volumen nimmt ab. Über Finasterid haben wir mehrfach berichtet (6). Dutasterid wurde nicht gegen Finasterid getestet, sondern gegen Plazebo. Die Ergebnisse mit 0,5 mg Dutasterid sind offenbar ganz ähnlich wie mit Finasterid. Dutasterid ist allerdings etwas billiger und hat sich daher zur Behandlung der stark hypertrophierten Prostata rasch durchgesetzt.
Emtricitabin (Emtriva®) ist ein Analogpräparat aus der Gruppe der Nukleosid-Reverse-Transkriptase-Inhibitoren für die HIV-Therapie. Es unterscheidet sich von den gängigen Substanzen Lamivudin, Tenofovir (Viread®) und Didanosin (Videx®) nur wenig, auch nicht im Preis.
Über die einführungsrelevanten Studien von Enfuvirtid (Fuzeon®) haben wir eingehend berichtet (7). Es handelt sich um einen sogenannten Fusionsinhibitor, der bei HIV-infizierten Patienten mit „Multidrug resistance” eingesetzt werden kann. Die Häufigkeit resistenter Viren nimmt zu. Enfuvirtid ist daher eine sehr erwünschte Innovation, deren Preis vom Hersteller allerdings so hoch kalkuliert ist, dass sie nicht überall eingesetzt werden kann, wo sie gebraucht wird.
Escitalopram (Cipralex®) ist das aktive, linksdrehende Enantiomer des seit Jahren verkauften Serotonin-Wiederaufnahme-Hemmers und Antidepressivums Citalopram (z.B. Cipramil®). Hier wird ein häufig erfolgreicher Trick erneut angewandt, nämlich das aktive Enantiomer auf den Markt zu bringen, wenn der Patentschutz der razemischen Muttersubstanz ausläuft, z.B. Nexium® für Antra® (vgl. 8). Beide Substanzen sind nach der Meinung sorgfältiger Analysten therapeutisch gleichwertig (9). Die Tagesdosis von Citalopram als Generikum kostet etwa 0,90 EUR, die Tagesdosis von Cipralex® 1,28 EUR. Wir wundern uns, dass Cipralex® trotzdem in Deutschland 27000mal zu Lasten der gesetzlichen Krankenkassen verordnet worden ist.
Laronidase (Aldurazyme®) ist ein Enzymersatz zur Therapie der Mukopolysaccharid-Speicherkrankheit (Hurler-Syndrom, Ullrich-Scheie-Syndrom). Jahrestherapiekosten 185000-600000 EUR. Miglustat (Zavesca®) hemmt ein Enzym, das den Substratanfall beim M. Gaucher vermindert. Jahrestherapiekosten 117000 EUR. Die Preise dieser Substanzen werfen spezielle ethische Probleme auf, deren Betrachtung den Rahmen dieser Übersicht sprengt.
Norelgestromin ist ein neuartiges Gestagen, das zusammen mit Ethinylestradiol erstmals eine hormonale Kontrazeption mit Hilfe eines Pflasters möglich macht (Evra®). Diese Methode ist zwar sicher, aber nicht sicherer als die Kontrazeption durch Tabletteneinnahme. Auch die UAW dürften ähnlich sein. Norelgestromin ist der aktive Metabolit von Norgestimat, das als Gestagenkomponente z.B. in dem hormonalen Kontrazeptivum Cilest® enthalten ist. Langzeitbeobachtungen fehlen. Ein vermindertes Thromboembolie-Risiko ist unwahrscheinlich (15). Ethinylestradiol ist chemisch sehr stabil, wird kaum abgebaut und führt daher zu Umweltbelastungen. Die Kosten von Evra® sind fast doppelt so hoch wie die einer niedrig dosierten oralen Kontrazeption, z.B. Leios®.
Pegfilgrastim (Neulasta®) ist ein kovalentes Konjugat des rekombinanten humanen Granulozyten-Kolonien stimulierenden Faktors (G-CSF) mit hochmolekularem Polyethylenglykol (PEG). Durch die „Pegylierung” wird die Halbwertszeit verzehnfacht im Vergleich zum Filgrastim (Neupogen®). Pegfilgrastim wird daher bei Chemotherapie-Schemata mit zeitlich begrenzter Dauer der Neutropenie nur einmal als s.c. Injektion ca. 24 Stunden nach der zytotoxischen Chemotherapie angewendet. In einer randomisierten, doppeltblinden kontrollierten klinischen Studie bei Patientinnen mit Hochrisiko-Mammakarzinom, die zum Teil mit Zytostatika vorbehandelt waren, war eine einmalige Injektion von Pegfilgrastim 100 µg/kg pro Chemotherapiezyklus bei vergleichbarem Nebenwirkungsprofil ebenso wirksam (primärer Endpunkt: Dauer der schweren Neutropenie Grad 4) wie Filgrastim (tägliche Injektionen von 5 µg/kg/d). Überzeugende Ergebnisse, dass Pegfilgrastim signifikant seltener mit febriler Neutropenie assoziiert ist als Filgastrim, liegen bisher nicht vor. Auch ein Vergleich der Therapiekosten von Pegfilgrastim und Filgrastim ist anhand der bisher durchgeführten klinischen Studien nicht sicher möglich, da Filgrastim in diesen Studien länger als klinisch notwendig (für 12-14 Tage oder bis zu einem Anstieg der absoluten Neutrophilenzahlen ≥ 10 x 109/l) verabreicht wurde. Die Kosten der einmaligen Gabe von Pegfilgrastim (1524 EUR) entsprechen etwa den Kosten für zehn Dosen Filgrastim 300 µg. Ob durch Pegfilgrastim eine Kostenreduktion erreicht werden kann, hängt somit von dem Ausmaß der Myelosuppression der Chemotherapie und den benötigten Filgrastim-Dosen ab. Aufgrund der vereinfachten Therapie und dem weitgehenden Ausschluss von Dosierungsfehlern ist das langwirkende Pegfilgrastim als Fortschritt in der Behandlung Zytostatika-bedingter Neutropenien bei bestimmten Chemotherapie-Schemata anzusehen. Zur Indikationsproblematik vgl. (10). Aufgrund unzureichender Daten wird Filgrastim bei Kindern und Jugendlichen unter 18 Jahren nicht empfohlen.
Pegvisomant (Somavert®), ein neuer Wachstumshormon-Rezeptor-Antagonist, korrigiert die erhöhten Plasmakonzentrationen von IGF I (dem eigentlichen Wachstumsfaktor) bei Akromegalie mit großer Zuverlässigkeit. In der Therapie ist Somavert aber zunächst, z.B. wegen des ungeklärten Einflusses auf die Größe des Hypophysentumors, nur ein Reservemedikament hinter Operation, Bestrahlung der Hypophyse und Somatostatin-Analoga (11).
Tadalafil (Cialis®) und Vardenafil (Levitra®) wurden zu Sildenafil (Viagra®) als zwei weitere Phosphodiesterase-5-Hemmer zur Behandlung der erektilen Dysfunktion eingeführt. Sie unterscheiden sich nicht im Wirkungs- und Nebenwirkungsprofil und in auffälliger Weise auch nicht im Preis pro Dosis. Sie unterscheiden sich im Wirkungsablauf. Die Wirkung von Tadalafil tritt erst nach vier Stunden ein, hält aber 36 Stunden an. Das ist kein Vorteil, wenn man die möglichen Nebenwirkungen bedenkt (z.B. Blutdruckabfall, Priapismus u.s.w.). Vardenafil entspricht dem Sildenafil.
Teriparatid (Forsteo®) ist ein synthetisches Fragment des humanen Parathormons (PTH) mit den N-terminalen Aminosäuren 1-34. PTH hat bei intermittierender s.c. Gabe – als intaktes PTH (1-84) oder als PTH-Fragment (1-34) – osteoanabole Effekte, besonders am trabekulären Knochen. In einer Studie fand sich im Vergleich zu Plazebo eine deutliche Reduktion neuer WK-Frakturen. Hinsichtlich nicht-vertebraler Frakturen war der Effekt von PTH geringer. In zwei kürzlich veröffentlichten Studien zeigte sich, dass die Kombination von PTH mit dem Bisphosphonat und Knochenresorptions-Hemmer Alendronat keinen zusätzlichen Effekt auf die Knochendichte gegenüber PTH alleine hat. In der Tier-Toxikologie sind bei Ratten Osteosarkome aufgefallen. Die Herstellerfirma hat die klinischen Studien abgebrochen. Die Anwendungsdauer ist auf 18 Monate begrenzt. Ein weiterer Nachteil ist der sehr hohe Preis. Als ultima ratio kann aber PTH bei einigen Patienten angezeigt sein (12).
Auch bei Valdecoxib (Bextra®), dem vierten Vertreter der selektiven COX-2-Inhibitoren, stehen wie bei Rofecoxib den Wirkungen ernste UAW gegenüber. In zwei randomisierten plazebokontrollierten Studien wurden nach koronaren Bypass-Operationen unter Valdecoxib dreimal mehr kardiovaskuläre Komplikationen beobachtet (16). Darüberhinaus fielen in Post-marketing-Beobachtungen andere schwere UAW auf (Angioödem, anaphylaktischer Schock), die ebenso wie die kardiovaskulären jetzt in der Fachinformation aufgeführt sind. Die EMEA will nach der Marktrücknahme von Vioxx® jetzt alle Coxibe erneut auf ihre kardiovaskuläre Sicherheit überprüfen. Bis dahin sollten sie bei Patienten mit Arteriosklerose nicht verordnet werden, sondern nur bei jüngeren Menschen mit Unverträglichkeit für andere nicht-steroidale Antiphlogistika. Über die auch im Jahr 2003 anhaltend häufigen Verordnungen kann man sich allein angesichts des vergleichsweise hohen Preises auch im Nachhinein nur wundern.
Dibotermin alfa (Inductos®) ist ein Knochen-Wachstumsfaktor, der nach Bindung an Oberflächenrezeptoren von Mesenchymzellen die Neubildung von Knochen induziert. Er wurde zur Unterstützung der Heilung offener Tibiafrakturen zugelassen. Er wird während der Operation in einer Matrix direkt auf die Frakturlinie aufgebracht. In einer Einfachblindstudie an 450 Patienten fanden sich eine verkürzte Heilungsdauer der Frakturen und seltener Sekundärinfektionen. Bei geblindeter, radiographischer Beurteilung der Heilungsdauer ergab sich aber kein überzeugender Unterschied. Vor dem Einsatz von Dibotermin alfa in der traumatologischen Routine müssen wohl weitere Studien abgewartet werden.
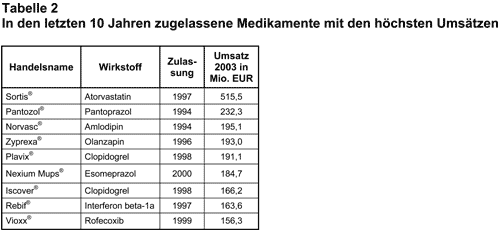
Verordnung neuer Medikamente im Jahr 2003: Valdecoxib ist das im Jahre 2003 zugelassenene Medikament, das mit 430000 Verordnungen und einem Umsatz von 18,2 Mio. EUR wirtschaftlich am erfolgreichsten war. Cipralex (273000 Verordnungen) und Avodart (232000 Verordnungen) machten ebenfalls schon im ersten Jahr hohe Umsätze, nämlich 2,3 bzw. 2,9 Mio. EUR. Bei allen dreien handelt es sich um Analogpräparate, für die es preiswerte Alternativen gegeben hätte. Auch auf der Liste der umsatzstärksten Neuzulassungen der letzten zehn Jahre finden sich überwiegend Analogpräparate (s. Tab. 2), die ganz überwiegend ohne therapeutischen Nachteil hätten ausgetauscht werden könnten. So wurde im Jahre 2003 Simvastatin als Generikum verfügbar. Das hätte sich wie ein Erdrutsch auf die Verordnungshäufigkeit der übrigen Statine auswirken können. Er ist jedoch ausgeblieben. Atorvastatin hatte dagegen 2003 weltweit einen Umsatzzuwachs von 14% auf 10,3 Mrd. US $.
Die neu auf den Markt gekommenen und „erfolgreichen” Arzneimittel sind überwiegend Analogpräparate (Tab. 2). Sie entwickelten sich mit einer Steigerung des Umsatzes von 21,5% stärker als der übrige Markt (plus 6%; 1). Würden Ärzte (und Partienten) nicht pharmakoökonomisch unsinnige Neueinführungen einsetzen, sondern die in Wissenschaft und Erfahrung bewährten „Muttersubstanzen”, hätten 2 Mrd. EUR eingespart werden können. Das Marketing der Firmen ist offenbar erfolgreich und darf daher auch teuer sein. Wichtige Informationsträger sind die Pharmareferenten, die Information, Werbung und anderes in die Praxen bringen, um das Verordnungsverhalten zu beeinflussen. Allein die Referenten von Pfizer, MSD und AstraZeneca machten während des Jahres 2003 insgesamt 25 Mio. Besuche. Dabei wurde sicher nicht nur über die Analogpräparate gesprochen. Die Besuche kosteten 2 Mrd. EUR (13) und dürften sich gelohnt haben. Vielleicht würde dem Aberglauben an neue Substanzen entgegengewirkt, wäre auf den Packungen – wie von vielen oft gefordert und in Großbritannien üblich – ein Warnhinweis gedruckt, der daran erinnert, dass über die UAW und damit das Preis/Leistungs-Verhältnis neuer Substanzen noch wenig bekannt ist.
Folgende Substanzen sind im Jahre 2003 als Generika neu auf den Markt gekommen: Lovastatin, Simvastatin, Cefixim, Gabapentin, Fluconazol, Moxonidin und Opipramol. 54% aller Verordnungen im Jahre 2003 betrafen Generika; das sind 2% mehr als im Vorjahr. Der Umsatz auf dem Generikamarkt ist allerdings seit 1993 nicht gewachsen, sondern hat von 32% auf 30% abgenommen. Die Teuerung fand bei den neuen Arzneimitteln statt. Durch die Verordnung von Generika sind im Jahre 2003 3,4 Mrd. EUR eingespart worden. Das Einsparvolumen hätte noch wesentlich größer sein können, wäre das jeweils preiswerteste Generikum verordnet worden. In manchen Praxen wird Software eingesetzt, die von Herstellern der Generika kostenlos zu Verfügung gestellt wird. Die Programme sind manipuliert: Für den Ausdruck der Rezepte wird das Präparat der eigenen Firma als erstes empfohlen. Die Kassenärztliche Bundesvereinigung will sich nach den Worten des 2. Vorsitzenden, Dr. L.R. Hansen, mit Priorität diesem Übel widmen (13).
Entwicklungen im Jahre 2004: Verschiedene Krankenkassen haben über die Auswirkungen des GKV -Modernisierungsgesetzes (GMG) auf die Verordnungen von Arzneimitteln berichtet. Die Barmer Ersatzkasse veranstaltete im Dezember 2004 ein Symposion zu diesem Thema (13). Folgende Punkte wurden herausgestellt: Die Verordnung nicht-rezeptpflichtiger Arzneimittel ist um 67% zurückgegangen (Packungen und Tagesdosierungen) seitdem sie – bis auf Ausnahmen – nicht mehr erstattungsfähig sind. Die Verordnung rezeptpflichtiger Packungen ist um 3,5% zurückgegangen, die der Tagesdosierungen hat um 3,6% zugenommen. Es werden also größere Packungen verordnet. Eine Substitution rezeptfreier Arzneimittel durch verordnungspflichtige und damit erstattungsfähige hat es nicht in nennenswertem Ausmaß gegeben. So hat sich z.B. zwar Dutasterid, wie oben gezeigt, stark entwickelt, aber nicht in demselben Ausmaß wie pflanzliche Prostatamittel nicht mehr verordnet werden können. Das Verordnungsverhalten ist also rationaler gewesen als manche Auguren befürchtet hatten. Eine Ausnahme sind die Antiallergika. Für die Molekülvarianten Desloratadin und Levocetirizin wurden 2,8 Mio. EUR ausgegeben, obwohl Loratadin und Cetirizin als Generika für die Hälfte des Preises zur Verfügung stehen (14). Auch die Coxibe hatten im Jahre 2004 bis zur Marktrücknahme von Vioxx noch einen erheblichen Umsatzzuwachs, der der Effektivität des Marketings und der kritiklosen Gutgläubigkeit vieler Ärzte zuzuschreiben ist. Denn zumindest die unabhängigen Arzneimittelzeitungen in aller Welt hatten seit der Einführung dieser Präparate darauf hingewiesen, dass diese sich von anderen nicht-steroidalen Antiphlogistika insgesamt und im Wesentlichen durch einen viel höheren Preis unterschieden, und dass daher der kometenhafte Aufstieg nicht nachvollziehbar sei. Auch bei Protonenpumpen-Hemmern und bei Statinen hat sich im Jahre 2004 trotz aller Information die Werbung durchgesetzt und den endgültigen Übergang von den Originalpräparaten zu Generika verhindert. Die Millionenbeträge könnten an anderer Stelle sinnvoller ausgegeben werden. Vor diesem Hintergrund ist es nicht verwunderlich, dass z.B. auf dem schon genannten Symposion der Barmer Ersatzkasse (13) die Wirksamkeit von Steuerungsinstrumenten diskutiert wurde, nämlich:
· Festbetragsregelungen,
· Preiskorrekturen, die an vergleichende Bewertung des Nutzens gebunden sind,
· wirtschaftliche Arzneimittelversorgung bei Hausarztmodellen und anderen integrierten Versorgungen,
· intensivere Wirtschaftlichkeitsprüfungen in den Praxen,
· Verbot manipulierender Praxissoftware.
Literatur
- Schwabe, U., und Paffrath, D.: Arzneiverordnungs-Report 2004. Springer, Berlin, Heidelberg, New York.
- AMB 2004, 38, 51.
- AMB 2001, 35, 41.
- AMB 1999, 33, 71a.
- de Witt, R., et al.: J. Clin. Oncol. 2003, 21, 4105.
- AMB 1998, 32, 23a; 1999, 33, 72b; 2003, 37, 66.
- AMB 2004, 38, 9.
- AMB 2003, 37, 1.
- Dyer, O.: Brit. Med. J. 2003, 326, 1004.
- AMB 1999, 33, 46.
- AMB 2002, 36, 13a.
- AMB 2004, 38, 33.
- Glaeske, G.: Evidenz und Effizienz in der Arzneimitteltherapie. Barmer Ersatzkasse, Symposion 2004.
- AMB 2004, 38, 63b.
- AMB 2003, 37, 84.
- Ray, W.A., et al.: N. Engl. J. Med. 2004, 351, 2767.