Zusammenfassung: In der aktuellen SPRINT-Studie mit mehr als 9.000 älteren hypertensiven Patienten mit erhöhtem kardiovaskulären Risiko ergab sich bei intensiver medikamentöser Senkung des Blutdrucks (Zielwert systolisch < 120 mm Hg) im Vergleich zu einer leitlinienkonformen Blutdrucksenkung (Zielwert systolisch < 140 mm Hg) eine signifikante Reduktion klinischer Endpunkte, einschließlich der Letalität. Dem stehen deutlich häufigere Nebenwirkungen gegenüber: Hypotonie, Synkopen, Elektrolytverschiebungen, Nierenversagen. Wegen der Ausschlusskriterien, z.B. Diabetes mellitus und Zustand nach Schlaganfall, sind die Ergebnisse in der Praxis nur eingeschränkt auf typische hypertensive Patienten mit hohem Risiko übertragbar. Ergebnisse aus anderen Studien, in denen eine zu intensive Blutdrucksenkung zu vermehrten Nebenwirkungen und höherer Letalität führte, mahnen zur Vorsicht bei der Umsetzung. Künftige Studien und Leitlinien zur Behandlung der Hypertonie werden mehr als bisher individuelle Kofaktoren (Alter, Komorbiditäten, Gebrechlichkeit, Polypharmakotherapie, Präferenz des Patienten) berücksichtigen müssen.
Einleitung: Die Senkung hypertensiver Blutdruckwerte reduziert die Inzidenz von Herzinsuffizienz, Schlaganfall, Koronarer Herzkrankheit (KHK) und chronischen Nierenerkrankungen und dies unabhängig von Alter, Geschlecht, ethnischer Zugehörigkeit und Schweregrad der Hypertonie. Darüber besteht internationaler Konsens. Uneinigkeit besteht unter Experten jedoch darüber, welche Blutdruckwerte therapeutisch anzustreben sind. Seit mehr als einem Jahrzehnt galt als Ziel < 140/90 mm Hg für die meisten Hypertoniker und < 130/80 mm Hg für Diabetiker und Patienten mit chronischen Nierenerkrankungen (1). 2014 wurde vom Eighth Joint National Committee der systolische Zielblutdruck für Menschen ≥ 60 Jahre auf der Basis randomisierter kontrollierter Studien auf 150 mm Hg angehoben (2). Die American Heart Association und das American College of Cardiology empfahl ursprünglich 130/80 mm Hg für Personen mit hohem Risiko für KHK und < 120/80 mm Hg für Patienten mit Herzinsuffizienz, änderte jedoch die Empfehlungen in diesem Jahr auf < 140/90 mm Hg für die meisten Patienten mit KHK und < 150/90 mm Hg für Menschen > 80 Jahre (3). Es lag also nahe, diese unterschiedlichen Leitlinien-Empfehlungen in einer neuen Studie zu überprüfen.
SPRINT-Studie: Wegen eines unerwartet signifikant positiven Therapieeffekts wurde im vergangenen August das Systolic Blood PRessure Intervention Trial (SPRINT) vorzeitig abgebrochen. Die Fachwelt hat auf die endgültigen Resultate gewartet (4). Diese wurden nun Anfang November auf dem Jahreskongress der American Heart Association (AHA) präsentiert – begleitet von einem ungewöhnlich großen Echo in der Fachpresse: Neben der fast zeitgleichen Publikation im N. Engl. J. Med. (5) gab es in derselben Ausgabe zwei Editorials (6, 7) und einen Perspektivartikel (8) sowie außerdem einen kommentierenden Artikel im J. Am. Coll. Cardiol. und ein Editorial und drei Kommentare in der Zeitschrift Hypertension (z.B. 9). Es wird allgemein angenommen, dass die Ergebnisse der SPRINT-Studie die Hypertoniebehandlung verändern werden.
Methodik: Die von den US-amerikanischen National Institutes of Health (NIH) unter Führung des National Heart, Lung, and Blood Institute (NHLBI) finanzierte, multizentrische Studie schloss Hypertoniker > 50 Jahre mit systolischen RR-Werten von 130-180 mm Hg und erhöhtem kardiovaskulärem Risiko ein – aber ohne Diabetes, Schlaganfallanamnese, Herzinsuffizienz oder kurz zurückliegendem akutem Koronarsyndrom (ACS; s. Tab. 1).
Die Patienten erhielten randomisiert, nicht verblindet („open label“) eine antihypertensive Arzneimitteltherapie mit einem systolischen Blutdruck-Zielwert von < 120 mm Hg ("Intensiv") vs. leitlinienkonform < 140 mm Hg ("Standard"). Die Auswahl der Arzneimittel wurde den behandelnden Ärzten und ihren Patienten überlassen. Der kombinierte primäre Endpunkt umfasste Myokardinfarkt und andere akute Koronarsyndrome, Schlaganfall, akut dekompensierte Herzinsuffizienz und kardiovaskulären Tod. In den ersten drei Monaten erfolgten monatliche, danach 3-monatliche Untersuchungen (RR-Messung in der Praxis, klinische Untersuchung, Labor, Fragebögen zu Endpunkten). Die geplante mittlere Nachbeobachtungszeit betrug 5 Jahre.
Ergebnisse: 9.361 Personen aus 102 Zentren wurden von November 2010 bis März 2013 eingeschlossen und 1:1 randomisiert mit folgenden Basischarakteristika in beiden Gruppen (auszugsweise): mittleres Alter 68 Jahre; Alter > 70 Jahre ca. 28%; Frauen ca. 36%; Afroamerikaner ca. 30%; mittlerer BMI 30 kg/m2; mittlerer Ausgangs-RR: 140/78 mm Hg; Zahl der Antihypertensiva bei Eintritt in die Studie 1,8/Patient; unbehandelte Patienten 10%; Statin-Therapie: 43%; ASS-Therapie: 52%.
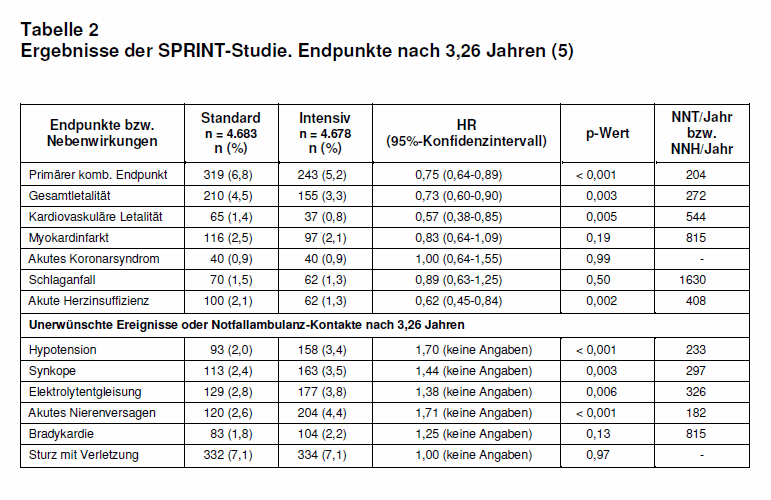
Patienten der Intensiv-Gruppe wurden in Folge im Durchschnitt mit 2,8 Antihypertensiva behandelt, Patienten der Standardgruppe weiterhin mit 1,8. Nach einem Jahr lag der Blutdruck in der Intensivgruppe im Mittel systolisch bei 121,4 mm Hg und diastolisch bei 68,7 mm Hg, in der Standard-Gruppe systolisch bei 136,2 mm Hg und diastolisch bei 76,3 mm Hg. Nach einer mittleren Nachbeobachtungszeit von 3,26 Jahren (statt der geplanten 5 Jahre) verfügte das NHLBI wegen einer unerwartet niedrigeren Letalität in der Intensiv-Gruppe den vorzeitigen Abbruch der Studie. Die Auswertung ergab zu diesem Zeitpunkt eine signifikante Reduktion des kombinierten Studienendpunkts in der Intensiv-Gruppe sowie der Gesamtletalität, der kardiovaskulären Letalität und der akuten Herzinsuffizienz (s. Tab. 2). Die Effekte waren in allen vor Studienbeginn definierten Subgruppen konstant. Schwere unerwünschte Ereignisse (UAW) wie Hypotension, Synkope, Elektrolytentgleisung, akute Niereninsuffizienz waren in der Intensiv-Gruppe häufiger. Hinsichtlich Bradykardien und Stürzen mit Verletzungsfolgen gab es hingegen keine Unterschiede (s. Tab. 2). In der Altersgruppe > 75 Jahre traten Nebenwirkungen unter Intensivtherapie überraschenderweise nicht häufiger auf als bei jüngeren Patienten.
Diskussion: Autoren und Kommentatoren sind sich einig, dass die Vorteile der intensiveren medikamentösen RR-Senkung mit einem Zielwert von systolisch < 120 mm Hg statt < 140 mm Hg in der SPRINT-Studienpopulation die häufigeren Nebenwirkungen aufwiegen. Dem ist im Grundsatz nicht zu widersprechen, wenn auch die Risikoveränderungen absolut verhältnismäßig gering sind. Dadurch ergibt sich eine hohe jährliche Number-Needed-To-Treat (NNT) bzw. Number-Needed-To-Harm (NNH; s. Tab. 2). Diese Effekte zwingen nach unserer Einschätzung nicht dazu, jetzt sofort die bisherigen Standards zu verlassen. Es ist jedoch davon auszugehen, dass die Ergebnisse der SPRINT-Studie in Form von Empfehlungen zu niedrigeren RR-Zielwerten Eingang in künftige Leitlinien finden werden.
Kritikpunkte an der SPRINT-Studie sind: Die fehlende Verblindung birgt naturgemäß ein hohes Risiko für einen Performance- und Beobachtungsbias. Eine vollständige Verblindung ist allerdings bei einer Studie, die ausschließlich Therapiezielwerte miteinander vergleicht, weder für Patienten noch für die einschließenden und nachuntersuchenden Ärzte und Studienassistenten praktikabel. Auch schränken die Ein- und Ausschlusskriterien die Übertragbarkeit der Studienergebnisse auf eine Hochrisikopopulation von Hypertonikern im Praxisalltag ein (Selektionsbias). Manche Kommentatoren sprechen deshalb kritisch von einem „SPRINT-spezifischen“ Effekt (9). Hinzu kommt eine möglicherweise unzureichende Begleittherapie: Den Patienten wurde in beiden Gruppen zwar zu einer begleitenden Lebensstil-Modifikation geraten, diese war aber nicht in das antihypertensive Management integriert – trotz eines erhöhten mittleren BMI von 30 kg/m2 in der Studienpopulation. In Anbetracht des kardiovaskulären Risikoprofils verwundert auch der relativ geringe Anteil der Patienten, die ASS (52%) oder ein Statin einnahmen (43%).
Positiv hervorzuheben ist in der SPRINT-Studie – im Vergleich zu anderen Hypertoniestudien – dass verhältnismäßig viele sonst unterrepräsentierte Patienten eingeschlossen wurden: ältere Hypertoniker, Frauen und Afroamerikaner. Subgruppen, die mehr als andere von der intensiveren RR-Senkung profitierten, waren: Patienten > 75 Jahre, Patienten ohne vorbestehende kardiovaskuläre Erkrankung oder Niereninsuffizienz (CNI) und, besonders interessant, Patienten mit niedrigem Ausgangs-RR (untere Tertile: ≤ 132 mm Hg).
Nebenwirkungen waren in der Altersgruppe > 75 Jahre nicht häufiger als in der Gesamtpopulation. Zu Verschlechterungen der Nierenfunktion kam es in der Intensiv-Gruppe zwar häufiger (bei insgesamt niedrigeren Ereignisraten als erwartet), jedoch gab es „keinen Hinweis auf substanzielle bleibende Nierenschäden“ infolge des niedrigeren RR-Zielwerts. Eine relevante Verminderung der eGFR fand sich bei Patienten ohne vorbestehende CNI signifikant häufiger unter intensiver RR-Senkung als unter Standard-Therapie (1,21%/Jahr vs. 0,35%/Jahr).
Ein Kommentator gibt zu bedenken, dass RR-Zielwerte von < 120 mm Hg – insbesondere bei Patienten mit höheren Ausgangswerten (z.B. > 170 mm Hg) – erfahrungsgemäß nur schwer zu erreichen sind (9). Eine Senkung des derzeit geltenden Zielwerts von < 140 mm Hg auf < 120 mm Hg wäre mit einem deutlichen Mehraufwand verbunden. Fragen zur optimalen "intensiven" antihypertensiven Arzneimitteltherapie (z.B. idealer Zeitpunkt sowie Art und Dosierung einer Kombinationstherapie) und deren Erfolgskontrolle (z.B. Art und Ort der RR-Messungen, optimale Länge von Kontrollintervallen) werden jedenfalls wieder an Bedeutung gewinnen. Diese Aspekte waren etwas in den Hintergrund getreten angesichts "lockerer" Zielwerte in den aktuellen europäischen und US-amerikanischen Leitlinien ("< 140 mm Hg für alle" bzw. < 150/90 mm Hg für Patienten mit Polypharmakotherapie oder durch Nebenwirkungen gefährdete ältere Patienten > 60 bzw. > 80 Jahre; 10-12).
Eine wesentliche Grundlage der derzeit aktuellen Leitlinien ist die 2010 publizierte ACCORD-BP-Studie (5.509 Diabetiker mit Hypertonie, randomisiert zu Zielwert < 120 mm Hg vs. 140 mm Hg, kein vorgegebenes Therapieregime, nicht verblindet; vgl. 13, 14). Dabei handelte es sich um eine Substudie der ACCORD-Studie, in der bei 10.251 Diabetikern in einem doppelten 2x2-faktoriellen Design Strategien der Blutzucker-, Blutdruck- und Lipidtherapie verglichen wurden. Die SPRINT-Studie hat sich in ihrem Design an der ACCORD-BP-Studie orientiert. Anders als in SPRINT fanden sich in der ACCORD-BP Studie jedoch keine Unterschiede in den klinischen Endpunkten, abgesehen von einer nicht-signifikanten Senkung der Schlaganfallrate bei jedoch höherer Rate an Nebenwirkungen. Dies könnte auf unterschiedliche Pathomechanismen bzw. Krankheitsstadien bei den beiden Studienpopulationen hinweisen und bekräftigt den Wert einer differenzierten blutdrucksenkenden Therapie, je nach Komorbidität, Alter, Gebrechlichkeit oder vorhandener Polypharmakotherapie. Wie solche neuen und stärker an der klinischen Situation des Patienten orientierten Empfehlungen im Detail aussehen könnten, ist jedoch in Anbetracht der Ein- und Ausschlusskriterien der SPRINT-Studie und der widersprüchlichen Evidenzlage nicht einfach zu entscheiden.
Generell nun einen niedrigeren RR-Zielwert, d.h. < 120 mm Hg, für "SPRINT-Patienten" festzusetzen (bei insgesamt niedrigeren Ereignisraten als erwartet), erscheint uns jedenfalls bedenklich. Es gibt nämlich Beobachtungen, dass eine allzu intensive Blutdrucksenkung vermehrt mit kognitiver Dysfunktion und höherer Letalität assoziiert ist (15, 16).
Aufgrund der Einschlusskriterien kann die SPRINT-Studie keine Aussagen machen zu den optimalen Zielwerten bei Patienten < 50 Jahre, Diabetikern und zu bisher nicht therapiepflichtigen Personen mit RR-Werten zwischen 120 mm Hg und 140 mm Hg.
Literatur
- Chobanian,A.V., et al.: JAMA 2003, 289, 2560. Link zur Quelle Erratum: JAMA 2003, 290, 197.
- James,P.A., et al.: JAMA 2014, 311, 507. Link zur Quelle Erratum: JAMA 2014, 311,1809.
- Rosendorff,C., et al.: J. Am. Coll. Cardiol. 2015, 65, 1998. Link zur Quelle
- Topol, E.J. undKrumholz, H.M.: Link zur Quelle
- SPRINTResearch Group (Systolic blood PRessure INtervention Trial):N. Engl. J. Med. 2015, 373, 2103. Link zur Quelle
- Perkovic,V., und Rodgers, A.: N. Engl. J. Med. 2015, 373, 2175. Link zur Quelle
- Drazen,J.M., et al.: N. Engl. J. Med. 2015, 373, 2174. Link zur Quelle
- Chobanian,A.V.: N. Engl. J. Med. 2015, 373, 2093. Link zur Quelle
- Esler, M.: Hypertension 2015Nov 9. pii: HYPERTENSIONAHA.115.06735. Epub ahead of print.. Link zur Quelle
- Mancia, G., et al.: Eur. Heart J.2013, 34, 2159. Link zur Quelle
- James, P.A., et al.: JAMA 2014, 311,507. Link zur Quelle
- Weber, M.A., etal.: J. Clin. Hypertens. (Greenwich) 2014, 16, 14. Link zur Quelle
- Cushman, W.C., et al. (ACCORD BP = Actionto Control CardiOvascular Risk in Diabetes BloodPressure): N. Engl. J. Med. 2010, 362, 1575. Link zur Quelle
- AMB 2010, 44, 36. Link zur Quelle
- AMB 2015, 49, 20. Link zur Quelle
- AMB 2015, 49, 39. Link zur Quelle