Zusammenfassung: In den letzten zwei Jahren wurden erst in den USA und dann in Europa sechs neue Antibiotika für die i.v. Therapie zugelassen: Ceftobiprol, Telavancin, Dalbavancin, Oritavancin, Tedizolid (auch oral) sowie die Kombination Ceftozolan/Tazobactam. Diese Wirkstoffe sind keine Vertreter neuer chemischer Gruppen, sondern Weiterentwicklungen bekannter Wirkstoffgruppen wie Cefalosporine, Glykopeptide oder Oxazolidinone. Sie sind in erster Linie gegen Infektionen mit grampositiven Problemkeimen, insbesondere multi(Methicillin-)resistente Staphylokokken (MRSA) entwickelt worden (vgl. 1). Nur die weiterentwickelten Cefalosporine Ceftobiprol und Ceftozolan sind auch im gramnegativen Bereich gut wirksam, allerdings nicht gegen Extended-Spektrum Betalaktamase bildende Enterobakterien (ESBL). Die Zulassungsstudien waren auf Prüfung der Nicht-Unterlegenheit in der Wirksamkeit im Vergleich mit der jeweiligen Standardtherapie konzipiert. Die Vorteile der neuen Antibiotika sind insgesamt moderat, die Preise extrem hoch. Wie fast immer bei neuen Wirkstoffen lassen sich aus den relativ kleinen und kurz dauernden Zulassungsstudien die Wirksamkeit (verglichen mit therapeutischen Alternativen) und die Nebenwirkungen – somit das Nutzen-Schaden-Verhältnis – nicht zuverlässig abschätzen.
Antibiotika sind potenziell lebensrettende Arzneimittel, die entsprechend strenger Indikation möglichst gezielt eingesetzt werden müssen. Diese Forderung wird in der täglichen Praxis sowohl im ambulanten als auch im stationären Bereich nur unbefriedigend umgesetzt. Die Erfahrung von Infektiologen in größeren – auch universitären – Krankenhäusern zeigt, dass nur bei etwa 25% der angesetzten Antibiotikabehandlungen eine strenge und gezielte Indikation vorliegt. Ein solcher inadäquater Einsatz führt nicht nur zu unbefriedigenden therapeutischen Ergebnissen, sondern auch zu vermeidbaren Komplikationen und Nebenwirkungen, die sogar lebensbedrohlich sein können: Anaphylaktische Reaktionen, Hypersensitivitätssyndrom, Leber-, Nieren-, Knochenmarktoxizität, schwere neurologische Ausfälle, psychische Störungen sowie Infektionen mit Clostridien. Außerdem steigen durch unnötige und falsche Indikationen die Zahl und Verbreitung von Erregern mit komplexen Resistenzen gegen bisher klinisch wichtige Antibiotika (vgl. 2). Zudem ist immer zu bedenken, dass durch antibiotische Therapien auch Bakterien abgetötet werden, die für den gesunden Organismus wichtig sind (3).
Über die Probleme mit resistenten Keimen, z.B. MRSA und ESBL, wird seit Jahren viel diskutiert. Dabei werden von sogenannten Experten, im Chor mit den pharmazeutischen Unternehmern (pU), immer wieder neue Antibiotika und mehr Geld für die Entwicklung von Antibiotika gefordert. Durch die Einführung von „AntiBiotic Stewardships“ (ABS; 4, 5) und anderen Institutionen in Krankenhäusern und Gesundheitsbehörden soll der dringend notwendige rationale (evidenzbasiert restriktive und gezielte) Umgang mit Antibiotika etabliert werden. Solche interdisziplinären (z.B. Pharma-Dialog), zum Teil aber auch bürokratischen Initiativen und Institutionen mögen die gegenwärtig unbefriedigende Situation im Prinzip zwar verbessern helfen. Sie suggerieren aber eine trügerische Sicherheit und können auch versagen, wie eine australische Publikation zu ABS in einem Krankenhaus bei der (oft unsinnigen und überflüssigen) prophylaktischen Antibiotikatherapie vor chirurgischen Eingriffen kürzlich gezeigt hat (6). In dieser Studie waren die therapeutischen Informationen und Empfehlungen des ABS für die behandelnden Ärzte leicht zugänglich. Sie wurden vor Einführen des ABS zu 18% und danach nur zu 15% befolgt (p der Änderung: 0,568). Das spricht dafür, dass solche Maßnahmen nicht nur einfach angeordnet, sondern durch ständige und wohl auch kontrollierte Fortbildung verinnerlicht werden müssen. Zudem kommen solche edukativen Maßnahmen sehr spät im Laufe der ärztlichen Berufskarriere, nämlich erst dann, wenn in der Weiter- und Fortbildungszeit bereits eigenständig verantwortungsvolle therapeutische Entscheidungen zu treffen sind. Der rationale und verantwortungsvolle Umgang mit Antibiotika sollte deutlich früher, d.h. während der Ausbildung und Schulung junger Ärztinnen und Ärzte gelehrt und gelernt werden. Auch die frei zugänglichen Informationen und Empfehlungen des National Institute for Health and Clinical Excellence (NICE) im Internet haben bisher den Umgang mit der Verschreibung von Antibiotika in wesentlichen Punkten nicht verbessert (7, 8).
Bakterielle Resistenzen werden auch durch die Verwendung von (Reserve-) Antibiotika in der Massentierhaltung gefördert (vgl. 9). Dabei werden Antibiotika oft nicht nur dazu eingesetzt, kranke Tiere zu behandeln, sondern auch, um die angestrebten Mastgewichte aus Profitstreben schneller zu erreichen. Die Massentierhaltung und der Einsatz von (Reserve-)Antibiotika in diesem Bereich sind für uns Menschen gefährlich und müssen auch aus diesem Grund eingeschränkt werden. Im breiten Kampf gegen Infektionen und speziell gegen resistente Erreger werden künftig auch andere Strategien verfolgt werden müssen als nur die ständige Neuentwicklung von Antibiotika; dazu gehören Impfungen, Antikörper, Probiotika und Bakteriophagen (vgl. 10). Vor diesem Hintergrund ist es nicht nachvollziehbar, dass jede Zulassung eines neuen Antibiotikums als großer Fortschritt gepriesen wird.
In einem lesenswerten aktuellen Artikel kritisiert Peter Doshi, Mitherausgeber des BMJ, die beschleunigten und erleichterten Zulassungsverfahren von Antibiotika in den USA und außerdem die geringe Aussagekraft der Zulassungsstudien (11). Meist seien es nur kurz dauernde Nicht-Unterlegenheitsstudien mit nicht sehr aussagekräftigen Endpunkten und unzureichender statistischer Auswertung, die in dieser Form nicht belegen (können), dass ein neu zugelassenes Antibiotikum in der angegebenen Indikation besser oder sicherer ist als die bisher verfügbaren. Als Beispiel führt er die Zulassungsstudien von Telavancin an (s.u.), die ein Statistiker der Food and Drug Administration (FDA) genauer analysiert hat. Dabei stellte sich heraus, dass einige Patienten an dem Tag, an dem sie gemäß der Definition in der Studie als „geheilt“ klassifiziert waren, gestorben sind (11).
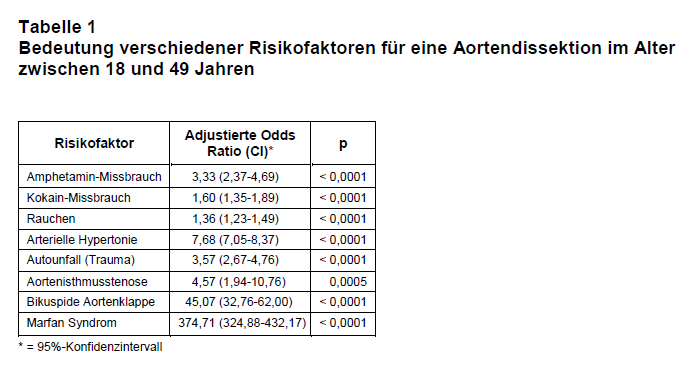
Im Folgenden sollen einige dieser neu zugelassenen Antibiotika kurz besprochen werden (s. Tab. 1).
Ceftobiprol (Zevtera®/Mabelio®) ist ein weiterentwickeltes Cefalosporin, das u.a. auch gegen MRSA und Vancomycin-resistente Stämme von Staphylococcus aureus (VRSA) wirksam ist. Gegen Erreger (überwiegend Enterobacteriaceae), die ESBL bilden (vgl. 2), ist es nicht wirksam und daher z.B. auch nicht für die Behandlung beatmungsassoziierter Pneumonien (Ventilator-assoziierte bakterielle Pneumonien = VABP) zugelassen. Die klinischen Heilungsraten betrugen in den Zulassungsstudien bei Patienten mit nosokomialer Pneumonie (außer VABP) ca. 78% (154 von 198 Patienten), im Vergleich zu ca. 76% (141 von 185 Patienten) in der Kontroll-Gruppe mit Ceftazidim plus Linezolid (12; Sponsor: Basilea Pharmaceutica). Das entsprach einer Nicht-Unterlegenheit. Bei Patienten mit VABP wurde die Nicht-Unterlegenheit dagegen nicht erreicht. Nebenwirkungen traten bei > 3% der Patienten auf: Übelkeit, Erbrechen, Durchfall, Reaktionen an der Infusionsstelle, Urtikaria (Allergie) und Geschmacksstörungen. Seltener waren Thrombozytopenie, Agranulozytose, Anaphylaxie, Clostridium-difficile-assoziierte Kolitis, Krampfanfälle, Panikattacken und Nierenversagen (12). Der Einsatz dieses Antibiotikums sollte sich also auf Patienten mit im Krankenhaus erworbener Pneumonie (ohne VABP) und Verdacht auf Problemkeime beschränken. Ceftobiprol muss dreimal pro Tag über 7-21 Tage verabreicht werden (s. Tab. 1). Preisgünstigere und ebenso wirksame Alternativen für solche Patienten könnten sein: Ceftazidim plus Vancomycin oder ein Carbapenem plus Vancomycin.
Telavancin (Vibativ®): Telavancin ist ein Derivat von Vancomycin und gehört wie Dalbavancin und Oritavancin (s.u.) zur Gruppe der Lipoglykopeptide. Die bakterizide Wirkung auf grampositive Bakterien (auch MRSA) beruht laut Hersteller auf einem dualen Mechanismus. Zum einen hemmt Telavancin, ähnlich wie Vancomycin, die Synthese der bakteriellen Zellwand und depolarisiert sie darüber hinaus, was letztlich zum Zelltod führt. Das unabhängige französische Arzneimittelbulletin Revue Préscrire veröffentlichte kürzlich einen Artikel mit der Überschrift: „Telavancin (Vibativ®). A vancomycin derivate, no more effective but more toxic“ (13). Dieser Beurteilung können wir uns anschließen. Schon mit der Zulassung des neuen Antibiotikums war der pU gezwungen, einen Rote-Hand-Brief herauszugeben, in dem über wichtige und gefährliche Nebenwirkungen (Nephro- und Reproduktionstoxizität, QT-Zeit-Verlängerung) informiert sowie über die Verwendung außerhalb der zugelassenen Indikation gewarnt wurde (14). Zu diesem Antibiotikum gab es mehrere kritikwürdige Studien (s.o. und 11) zur Nicht-Unterlegenheit gegenüber Vancomycin und Linezolid bei Haut- und Weichteilinfektionen sowie auch bei nosokomialen Infektionen (15-19; Hauptsponsor Theravance) und eine Metaanalyse (20). Das Nutzen-Risiko-Verhältnis von Telavancin bei der Behandlung von komplizierten Haut- und Weichteilinfektionen wurde vom Ausschuss für Humanarzneimittel (CHMP), dem EU-Komitee, das wissenschaftliche Gutachten für Zulassungsanträge von Arzneimitteln erstellt, negativ bewertet. Daher soll Telavancin bei dieser und anderen nicht zugelassenen Indikationen nicht angewendet werden. Telavancin wurde schließlich mit erheblichen Einschränkungen zugelassen, und zwar nur für die Behandlung von Patienten mit nosokomialer bakterieller Pneumonie (Hospital-Acquired Bacterial Pneumonia = HABP), einschließlich VABP, wenn diese nachgewiesen oder vermutet durch MRSA verursacht ist und wenn andere Antibiotikaoptionen nicht vorliegen oder erfolglos angewendet wurden (21). Bei Patienten mit eingeschränkter Nierenfunktion muss die Anfangsdosis entsprechend dem Grad der Einschränkung angepasst werden, ebenso bei Patienten, bei denen sich im Verlauf der Behandlung die Nierenfunktion verschlechtert. Generell muss in den ersten 3 bis 5 Tagen die Nierenfunktion täglich überprüft werden, danach alle 48-72 Stunden. Insgesamt dürfte Telavancin nur als letzte Option bei schweren nosokomialen Pneumonien auf Intensivstationen und bei VAP in Frage kommen, da die Nebenwirkungen erheblich sind und außerdem die Kosten hoch.
Dalbavancin (Xydalba®) und Oritavancin (Orbactiv®): Diese Lipoglykopeptid-Antibiotika wirken gegen grampositive Erreger, einschließlich MRSA. Beide haben eine hohe Bindung an Plasmaproteine (> 90%), was zu ihrer extrem langen Halbwertszeit beiträgt (> 200 h). Das hat einerseits den Vorteil, dass die Antibiotika nur wenige Male oder im günstigsten Fall nur einmal gegeben werden müssen, aber auch den Nachteil, dass bei Toxizität trotz Absetzen des Antibiotikums diese lange weiter besteht.
Dalbavancin und Oritavancin wurden auf der Basis zweier Studien 2014 in den USA und danach in Europa zu gelassen. In der DISCOVER-1 und -2-Studie (22; Sponsor: Durata Therapeutics) erhielten 288 Patienten mit Haut- und Weichteilinfektionen Dalbavancin als i.v. Infusion am Tag 1 und Tag 8. Diese Therapie wurde mit zweimal täglicher i.v. Infusion von Vancomycin bei 285 Patienten verglichen, ab dem 3. Tag auch optional mit Linezolid oral. Der primäre Endpunkt war das frühe Ansprechen der Infektion mit Rückgang der Rötung und Sistieren des Fiebers innerhalb von 48-72 h. In dieser Studie ergab sich für Dalbavancin keine Unterlegenheit (22). Häufigste unerwünschte Wirkungen waren Übelkeit, Kopfschmerzen und Durchfall. Unter Dalbavancin kam es zudem häufiger zu einem Anstieg der Leberenzyme als in der Vergleichsgruppe.
Wirksamkeit und akute Nebenwirkungen von Oritavancin wurden bei Patienten mit akuter Hautinfektion geprüft (23; Sponsor: Medicines Company). Eine Gruppe (n = 475) bekam eine Einmaldosis von 1.200 mg Oritavancin i.v., die Vergleichsgruppe (n = 479) zweimal Vancomycin i.v. (in der Regel zweimal 1 g, sonst nach therapeutischer Serumkonzentration und Nierenfunktion) für 7-10 Tage. Der zusammengesetzte Endpunkt bestand aus Abnahme des Areals der Hautrötung, dem Sistieren von Fieber und dem fehlenden Bedarf einer anschließenden Therapie mit einem weiteren Antibiotikum nach 48-72 h. In dieser Studie zur Therapie akuter Hautinfektionen war eine einmalige Dosis Oritavancin der Behandlung mit Vancomycin nicht unterlegen. Die häufigsten unerwünschten Nebenwirkungen waren Übelkeit, Kopfschmerzen und Durchfall.
Die Zulassung beider Antibiotika erfolgte für Haut- und Weichteilinfektionen. Eine Indikation sehen wir, wenn bei entsprechender bakterieller Resistenz oder Unverträglichkeiten keine andere antibiotische Option besteht. Eine solche Situation ist wahrscheinlich nur in < 5% aller komplizierten Haut- und Weichteilinfektionen in Deutschland gegeben. Die Frage, ob bei manchen Patienten durch Oritavancin – wegen der Einmaldosierung – der Krankenhausaufenthalt verkürzt werden kann, ist derzeit wegen fehlender Untersuchungen nicht zu beantworten. Nur dann wäre der hohe Preis im Vergleich zur Standardtherapie möglicherweise akzeptabel. Derzeit muss Dalbavancin über die Niederlande und Oritavancin über Großbritannien bezogen werden.
Tedizolid (Sivextro®): Tedizolid ist neben Linezolid ein weiterer Vertreter der Oxazolidione. Die antibiotische Wirkung dieser Wirkstoffklasse beruht auf der Hemmung der bakteriellen Proteinsynthese. Tedizolid ist auch gegen MRSA und Vancomycin-resistente Enterokokken/Staphylokokken wirksam und daher wie Linezolid zur Therapie komplizierter Haut- und Weichteilinfektionen geeignet. Tedizolid wurde in zwei Nicht-Unterlegenheitsstudien (Phase III) bei Hautinfektionen (Erysipel, Wundinfektionen) getestet (24, 25). Tedizolid (einmal täglich 200 mg oral; n = 332) wurde in der einen Studie (24; Sponsor: Trius Therapeutics) mit Linezolid verglichen (zweimal täglich 600 mg oral; n = 335). Die Behandlung dauerte 10 Tage. Der primäre Endpunkt der Studie war das klinische Ansprechen nach 48-72 h sowie 11-13 und 7-14 Tage nach Ende der Therapie. Tedizolid war in dieser Studie Linezolid nicht unterlegen. Der primäre Endpunkt wurde bei 81,6% der Patienten in der Tedizolid- und bei 79,4% in der Linezolid-Gruppe erreicht. Auch bei der Analyse von Subgruppen fand sich kein signifikanter Unterschied. In der Tedizolid-Gruppe reagierten weniger Patienten mit einem Abfall der Thrombozyten < 150.000/ml (4,9% vs. 10,8%; p = 0,0003). In der zweiten Studie (25; Sponsor: Cubist Pharmaceuticals) wurde die Wirksamkeit von Tedizolid i.v. (einmal täglich für 6 Tage) bei 332 Patienten mit akuten bakteriellen Haut- und Unterhautinfektionen mit Linezolid oral (zweimal täglich für 10 Tage) bei 334 Patienten verglichen. Tedizolid erwies sich als nicht unterlegen. Zu den häufigsten Nebenwirkungen gehörten Übelkeit (8%), Kopfschmerzen (6%), sekundäre Abszesse (4%), Durchfall (3%) und Erbrechen (3%). Diese waren geringfügig seltener als nach Linezolid.
Ceftolozan/Tazobactam (Zerbaxa®): Dies ist die Kombination eines neuen Cefalosporins mit dem Betalaktamase-Hemmstoff Tazobactam. Die gute Wirksamkeit der Cefalosporine in gramnegativen Bereich wird durch Tazobactam in den grampositiven Bereich erweitert. Die neue Kombination wurde in einer Nicht-Unterlegenheitsstudie bei 800 Patienten mit komplizierten Harnwegsinfektionen, einschließlich Pyelonephritis (n = 398) gegen Levofloxacin (n = 402) getestet (26; Sponsor: Cubist Pharmaceuticals). Der kombinierte Endpunkt war zusammengesetzt aus klinischer Heilung und mikrobiologischer Eradikation nach 5-9 Tagen. Die Heilungsrate in der Ceftolozan/Tazobactam-Gruppe betrug 76,9% vs. 68,4% in der Levofloxacin-Gruppe (Auswertung nach „intention to treat“). Das Studiendesign mit Behandlung der Patienten mit Levofloxacin in der Vergleichsgruppe – und auch die niedrige Heilungsrate – verwundert, denn in der Regel werden bei komplizierter Pyelonephritis bis das bakteriologische Ergebnis vorliegt Cefalosporine der 3. Generation oder – bei Verdacht auf ESBL – Carbapeneme eingesetzt. Zu den häufigsten Nebenwirkungen gehörten Kopfschmerzen, Verstopfung, Durchfall, Erbrechen und Übelkeit. Ein Anstieg der Leberwerte trat häufiger bei der neuen Kombination auf. Bei Patienten mit mäßig bis stark eingeschränkter Nierenfunktion bzw. bei hämodialysepflichtigen Patienten muss die Dosis angepasst werden. Patienten mit Immunsuppression oder schwerer Neutropenie waren von der Studie ausgeschlossen; es gibt also keine Daten dazu. Wir schätzen den zusätzlichen Nutzen dieser neuen Kombination als gering ein. Sie birgt auch die Gefahr erhöhter Toxizität durch zwei Inhaltsstoffe.
Literatur
- AMB 2015, 49,36 Link zur Quelle . AMB 2007, 41, 57. Link zur Quelle
- AMB 2013, 47,17 Link zur Quelle . 2010, 44, 76b Link zur Quelle . AMB 2007, 41,57. Link zur Quelle
- Blaser, M.: Nature 2011, 476,393. Link zur Quelle
- http://www.antibiotic-stewardship.de/ Link zur Quelle
- http://www.awmf.org/uploads/ tx_szleitlinien/092-001l_S3_Antibiotika_Anwendung_im_Krankenhaus_2013-12.pdf Link zur Quelle
- Knox, M.C., und Edyre,M.: Surg. Infect. (Larchmt.) 2015. Epub ahead of print. Link zur Quelle
- http://www.nice.org.uk/news/article/calls-for-nhs-to-curb- inappropriate-antibiotic-prescribing Link zur Quelle
- https://www.nice.org.uk/guidance/conditions-and-diseases/ infections/antibiotic-use Link zur Quelle
- AMB 2013, 47,17. Link zur Quelle
- Czaplewski, L., etal.: Lancet Infect. Dis. 2016, Jan. 12, in press. Link zur Quelle
- Doshi, P.: BMJ 2015, 350,h1453. Link zur Quelle
- Awad, S.S., et al.:Clin. Infect. Dis. 2014, 59, 51. Link zur Quelle
- Anonym: Prescrire Int.2015, 165, 257. Link zur Quelle
- http://www.akdae.de/Arzneimittelsicherheit/RHB/Archiv/2015/20150116.pdf Link zur Quelle
- Stryjewski, M.E., et al. (FAST): Clin. Infect. Dis. 2005, 40,1601. Link zur Quelle
- Stryjewski, M.E., et al.: Clin. Infect. Dis. 2008, 46, 1683. Link zur Quelle
- Rubinstein, E., et al.(ATTAIN = Assessment of Telavancin for Treatmentof hospital-AcquIred pneumonIa): Clin. Infect. Dis. 2011, 52, 31. Link zur Quelle
- Corey, G.R., et al.(ATTAIN = Assessment of Telavancin for Treatmentof hospital-AcquIred pneumonIa): Antimicrob. Agents Chemother. 2014, 58,2030. Erratum: Antimicrob. Agents Chemother. 2014, 58, 3581. Link zur Quelle
- Lacy, M.K., et al.(ATTAIN = Assessment of Telavancin for Treatmentof hospital-AcquIred pneumonIa): Clin. Infect. Dis. 2015, 81 Suppl. 2, S87. Link zur Quelle
- Polyzos, K.A., et al.:PLoS One 2012, 7, e41870. Link zur Quelle
- http://www.bfarm.de/SharedDocs/ Downloads/DE/Arzneimittel/ Pharmakovigilanz/Risikoinformationen/… Link zur Quelle
- Boucher, H.W., et al.(DISCOVER 1 und DISCOVER 2): N. Engl. J. Med. 2014, 370, 2169. Link zur Quelle
- Corey, G.R., et al.(SOLO I): N. Engl. J. Med. 2014, 370, 2180. Link zur Quelle
- Prokocimer, P., et al.(ESTABLISH-1): JAMA 2013, 309, 559. Link zur Quelle
- Moran, G.J., et al.(ESTABLISH-2): Lancet Infect. Dis.2014, 14, 696. Link zur Quelle
- Wagenlehner, F.M., et al. (ASPECT-cUTI): Lancet 2015, 385, 1949. Link zur Quelle